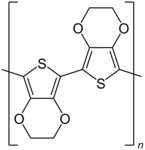
Poly-3,4-ethylendioxythiophen
| Strukturformel | |||||||
|---|---|---|---|---|---|---|---|
| |||||||
| Allgemeines | |||||||
| Name | Poly-3,4-ethylendioxythiophen | ||||||
| Andere Namen |
Kurzzeichen: PEDOT | ||||||
| CAS-Nummer | 155090-83-8 (PEDOT:PSS) | ||||||
| Monomere/Teilstrukturen | 3,4-Ethylendioxythiophen, | ||||||
| Art des Polymers | |||||||
| Kurzbeschreibung |
blaue Fasern (PEDOT:PSS)[1] | ||||||
| Eigenschaften | |||||||
| Aggregatzustand |
fest | ||||||
| Schmelzpunkt |
300 °C (Zersetzung) (PEDOT:PSS)[2] | ||||||
| Sicherheitshinweise | |||||||
| |||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||
Poly-3,4-ethylendioxythiophen (PEDOT, manchmal PEDT oder PDT) ist ein elektrisch leitfähiges Polymer auf Thiophenbasis. Es besteht aus 2,5-verknüpften 3,4-Ethylendioxythiophen-Einheiten (EDOT). Das Polymer besitzt ein vollständig durchkonjugiertes π-System der Doppelbindungen. Die automatisch eintretende „Dotierung“ während der Polymerisation zu PEDOT durch einen Dotant ermöglicht die Leitfähigkeit. Im oxidierten, leitfähigen Zustand werden die positiven Ladungen der Löcher in der konjugierten Kette durch Anionen kompensiert. PEDOT ist also ein Lochleiter.
Es gibt eine Vielzahl verschiedener PEDOT-Varianten und Darstellungswege, wobei hier PEDOT:PSS und PEDOT:Tos exemplarisch aufgrund ihrer signifikanten Unterschiede angesprochen werden.
Synthese
[Bearbeiten | Quelltext bearbeiten]Es muss zwischen PEDOT:PSS und anderen PEDOT-Varianten (wie PEDOT:Tos, PEDOT:Cl etc.) differenziert werden, da sich diese maßgeblich in ihren Darstellungsweisen und Prozessierungsschritten unterscheiden. Bei PEDOT:PSS handelt es sich um eine einsatzfertige wässrige Suspension, wobei PEDOT:Tos bzw. PEDOT:Cl nur auf einem Substrat als unlöslicher Film gebildet werden können. Wird EDOT in Lösung mit einem Oxidationsmittel versetzt, so fällt es als blauer Feststoff aus, der nach Abtrennung und Trocknung in elektrisch leitfähige PEDOT-Pellets gepresst werden kann.
Synthese von PEDOT:PSS
[Bearbeiten | Quelltext bearbeiten]PEDOT:PSS wird über die Oxidation von EDOT durch katalytische Mengen an Eisen(III)-sulfat in Wasser dargestellt. Die Reoxidation von Eisen wird durch Natriumpersulfat gegeben.[3] Zusätzlich wird der Polyelektrolyt Natrium-Polystyrolsulfonat zugegeben, der neben der Dotierung des PEDOTs auch für dessen Wasserlöslichkeit sorgt. Nachdem eine tiefblaue Dispersion entstanden ist, wird das Reaktionsgemisch mit Hilfe von Anionen- und Kationentauscherharzen aufgereinigt. Die wässrige PEDOT:PSS-Dispersion erreicht elektrische Leitfähigkeiten von ca. 0,1 – 2 S/cm. Durch hochsiedende Lösungsmittel wie DMSO oder Ethylenglycol wird die Leitfähigkeit massiv auf bis zu 500 S/cm erhöht.[4] Die Leitfähigkeitserhöhung ist auf die Separation von PEDOT und PSS bei der Filmbildung zurückzuführen. PSS an sich ist ein Isolator.
Synthese von PEDOT:Tos und Derivaten
[Bearbeiten | Quelltext bearbeiten]PEDOT:Tos wird durch die oxidative Polymerisation von EDOT mit Hilfe von Eisen(III)-tosylat hergestellt. Als Reaktionsmedium werden vorrangig unpolarere Lösungsmittel wie Butanol, Ethanol oder Acetonitril verwendet. Die Mischung aus EDOT, Eisen(III)-tosylat und Lösungsmittel wird mit Hilfe geeigneter Methoden wie Rotationsbeschichtung, Rakeln oder Ink Jetting auf ein Substrat aufgetragen. In der Hitze (70–100 °C) findet dann die oxidative Polymerisation statt. Die Nebenprodukte der Polymerisation werden durch Auswaschen mit Ethanol, Aceton oder Wasser aus dem Film gelöst. Es bleibt ein unlöslicher blauer Film zurück der in der Regel eine elektrische Leitfähigkeit zwischen 300 und 1400 S/cm aufweist (zum Vergleich: Quecksilber 10400 S/cm). Polymere Additive, vor allem Polyethylenglycole, führen zu solch hohen elektrischen Leitfähigkeiten.[5][6] Das Gegenion des Eisen(III)-salzes bestimmt hierbei das dotierende Anion, meist wird Tosylat gewählt, da es zu sehr hohen Leitfähigkeiten führt.
Bei der chemischen Präparation fällt es als unlöslicher, blauer Niederschlag aus. Ein geeignetes Oxidationsmittel ist Eisen(III)-chlorid (FeCl3). Wasser, Methanol, Ethanol, Acetonitril und andere polare Lösungsmittel können für die Synthese verwendet werden.[7] Bei der elektrochemischen Polymerisation von PEDOT scheidet es sich als blaue, elektrisch leitfähige Schicht auf der Anode ab. Um n Thiopheneinheiten zu verketten, werden idealerweise 2n − 2 Elektronen entzogen. Das PEDOT wird während der Polymerisation wegen seines im Vergleich zum EDOT niedrigeren Oxidationspotentials ebenfalls oxidiert. Der Oxidationsgrad liegt in der Regel zwischen 0,25 und 0,4. Folglich trägt jede dritte bis vierte Monomereinheit in der Polymerkette eine positive Ladung.[8] Zur Ladungskompensation werden deshalb während der Polymerbildung Anionen des Leitsalzes eingebaut. Das verwendete Gegenion bestimmt maßgeblich die Anordnung des entstehenden PEDOTs zueinander und somit auch die Polymereigenschaften.
Reaktionsmechanismus
[Bearbeiten | Quelltext bearbeiten]EDOT wird im ersten Reaktionsschritt zum Radikalkation oxidiert, das ein wesentliches Intermediat der oxidativen Polymerisation ist. Zwei Radikalkationen rekombinieren zum dimeren Dikation. Möglicherweise werden bereits während dieser Dimerisierung simultan zwei Protonen abgespalten.[9] Da das Oxidationspotential des nun gebildeten Dimers unter dem des Monomers liegt, wird es bevorzugt zum Radikalkation oxidiert. Durch äquivalente Polymerisationsschritte entsteht schließlich PEDOT, welches nicht als neutrales PEDOT anfällt, sondern durch überschüssiges Oxidationsmittel rasch dotiert wird.

Anwendung
[Bearbeiten | Quelltext bearbeiten]PEDOT wird in der Elektrotechnik für die Herstellung von Polymer-Aluminium- und Polymer-Tantal-Elektrolytkondensatoren, in der Sensortechnik, Solarzellentechnik und Mikrobiologie verwendet.[10] Großtechnisch wird PEDOT als Elektrodenmaterial in Kondensatoren verwendet.[11]
Elektrochromie
[Bearbeiten | Quelltext bearbeiten]In dünnen Schichten wird PEDOT als elektrochromes Material verwendet. Dabei ist das Polymer im oxidierten Zustand leicht himmelblau und nahezu durchsichtig. Im reduzierten Zustand wird die Absorption vor allem im Wellenlängenbereich zwischen 550 und 650 nm erhöht und PEDOT wird dunkelblau.[12]
PEDOT in der Thermoelektrik
[Bearbeiten | Quelltext bearbeiten]Seit 2008 gibt es ein gesteigertes Interesse an PEDOT in der Thermoelektrik als organisches Alternativmaterial zum anorganischen Bismuttellurid.[13] Es wurden schon Effizienzen erreicht, die denen von herkömmlichen Thermoelektrika nahe kommen. Jedoch konnten diese Bestwerte nur unter optimalen Laborbedingungen erzielt werden, was PEDOT bisher die wirtschaftliche Anwendung verwehrt.[14][15][16]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c Datenblatt Poly-(3,4-ethylendioxythiophen)-poly-(styrolsulfonat) bei Sigma-Aldrich, abgerufen am 17. Juni 2023 (PDF).
- ↑ Hyun Ju, Mihyun Kim, Jooheon Kim: Thermoelectric behavior of poly(3,4-ethylenedioxythiophene)/graphene composites depending on benzenesulfonate derivatives doped in polymer chains. In: Journal of Materials Science: Materials in Electronics. Band 26, Nr. 4, 25. Januar 2015, S. 2544–2554, doi:10.1007/s10854-015-2721-0.
- ↑ W. Lövenich, R. Hill: Polymer coatings containing conductive polymers. Google Patents, Februar 2011.
- ↑ Tsung-Che Tsai, Hsiu-Cheng Chang, Chun-Hua Chen, Wha-Tzong Whang: Widely variable Seebeck coefficient and enhanced thermoelectric power of PEDOT:PSS films by blending thermal decomposable ammonium formate. In: Organic Electronics. Band 12, Nr. 12, Dezember 2011, S. 2159–2164, doi:10.1016/j.orgel.2011.09.004.
- ↑ Olga Bubnova, Zia Ullah Khan, Abdellah Malti, Slawomir Braun, Mats Fahlman, Magnus Berggren, Xavier Crispin: Optimization of the thermoelectric figure of merit in the conducting polymer poly(3,4-ethylenedioxythiophene). In: Nature Materials. Band 10, Nr. 6, Juni 2011, S. 429–433, doi:10.1038/nmat3012.
- ↑ Elise M. Stewart, Manrico Fabretto, Mischa Mueller, Paul J. Molino, Hans J. Griesser, Robert D. Short, Gordon G. Wallace: Cell attachment and proliferation on high conductivity PEDOT–glycol composites produced by vapour phase polymerisation. In: Biomaterials Science. Band 1, Nr. 4, 5. März 2013, S. 368–378, doi:10.1039/C2BM00143H.
- ↑ S. Machida, S. Miyata, A. Techagumpuch: Chemical synthesis of highly electrically conductive polypyrrole. In: Synthetic Metals. Band 31, Nr. 3, 1989, S. 311–318, doi:10.1016/0379-6779(89)90798-4.
- ↑ Jürgen Heinze: Electronically conducting polymers. In: Eberhard Steckhan (Hrsg.): Electrochemistry IV. Topics in Current Chemistry. 152. Springer, Berlin/ Heidelberg 1990, ISBN 3-540-51461-9, S. 1–47, doi:10.1007/BFb0034363.
- ↑ Stephen V. Lowen, John D. Van Dyke: Mechanistic studies of the electrochemical polymerization of pyrrole: Deuterium isotope effects and radical trapping studies. In: Journal of Polymer Science Part A: Polymer Chemistry. Band 28, Nr. 3, 1990, S. 451–464, doi:10.1002/pola.1990.080280301.
- ↑ St. Kirchmeyer, D. Gaiser, H. C. Starck GmbH & Co KG: Elektronische Bauelemente: Extrem flach und flexibel
- ↑ Andreas Elschner, Stephan Kirchmeyer, Wilfried Lovenich, Udo Merker, Knud Reuter: PEDOT: Principles and Applications of an Intrinsically Conductive Polymer. CRC Press, 2010, ISBN 978-1-4200-6912-9.
- ↑ Anna Maier: Funktionelle Koordinationspolymerfilme aus Polyiminoarylenen mit Terpyridin … disserta Verlag, 2011, ISBN 3-942109-48-4, S. 10 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Prospero J. Taroni, Itziar Hoces, Natalie Stingelin, Martin Heeney, Emiliano Bilotti: Thermoelectric Materials: A Brief Historical Survey from Metal Junctions and Inorganic Semiconductors to Organic Polymers. In: Israel Journal of Chemistry. Band 54, Nr. 5-6, 1. Juni 2014, S. 534–552, doi:10.1002/ijch.201400037.
- ↑ Olga Bubnova, Zia Ullah, Abdellah Malti, Slawomir Braun, Mats Fahlman, Magnus Berggren, Xavier Crispin: Optimization of the thermoelectric figure of merit in the conducting polymer poly(3,4-ethylenedioxythiophene). In: Nature Materials. Band 10, Nr. 6, Juni 2011, S. 429–433, doi:10.1038/nmat3012.
- ↑ Teahoon Park, Chihyun Park, Byeonggwan Kim, Haejin Shin, Eunkyoung Kim: Flexible PEDOT electrodes with large thermoelectric power factors to generate electricity by the touch of fingertips. In: Energy & Environmental Science. Band 6, Nr. 3, 20. Februar 2013, S. 788–792, doi:10.1039/C3EE23729J.
- ↑ G.-H. Kim, L. Shao, K. Zhang, K. P. Pipe: Engineered doping of organic semiconductors for enhanced thermoelectric efficiency. In: Nature Materials. Band 12, Nr. 8, August 2013, S. 719–723, doi:10.1038/nmat3635.
