Maitotoxin-1
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Maitotoxin-1 | ||||||||||||||||||
| Andere Namen |
MTX-1 | ||||||||||||||||||
| Summenformel | C164H256Na2O68S2 | ||||||||||||||||||
| Kurzbeschreibung |
farbloser Feststoff[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 3425,86 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest[1] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
Maitotoxin-1, kurz MTX-1, ist eines von drei strukturell und biochemisch verwandten marinen Giften, die nach der tahitianischen Bezeichnung Maito für die Borstenzahndoktorfischart Ctenochaetus striatus benannt sind, in der es 1976 entdeckt wurde. Wenig später wurde es auch in einigen im Meer lebenden Einzellern gefunden, insbesondere der Art Gambierdiscus toxicus. Fische nehmen das Gift wahrscheinlich durch das Fressen dieser Dinoflagellaten auf. Eine unter anderem auf Maitotoxin-1 beruhende Lebensmittelvergiftung nach dem Verzehr entsprechender Fische wird als Ciguatera bezeichnet. In der biochemischen und physiologischen Forschung wird Maitotoxin-1 in Studien zu Ionenkanälen verwendet.
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Maitotoxin-1 als Reinsubstanz ist ein farbloser, amorpher Feststoff, der in Wasser sowie in Methanol, Acetonitril und Dimethylsulfoxid (DMSO) gut, in den meisten anderen organischen Lösungsmitteln jedoch kaum oder nicht löslich ist. Die primäre chemische Struktur wurde 1998 aufgeklärt. Das Molekül mit einer molaren Masse von 3425,86 Dalton (3425,86 g/mol) und der Summenformel C164H256Na2O68S2 besteht aus 32 Ringstrukturen, darunter 28 6-Ringe, drei 7-Ringe und ein 8-Ring, die zusammen mit 32 Etherbindungen und 28 Hydroxygruppen eine C142-Kette bilden. Vor der Entdeckung der Polytheonamide war Maitotoxin-1 das größte bekannte durch Biosynthese in einem lebenden Organismus entstehende Molekül, das nicht als Polymer aufgebaut ist.[4] Die dreidimensionale Struktur ist bekannt:[5]
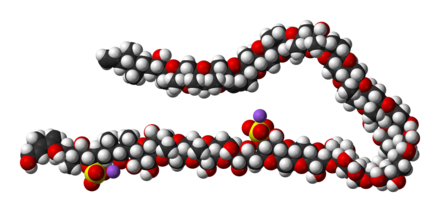
Trotz seiner komplexen Struktur ist Maitotoxin-1 im Gegensatz zu vielen anderen Tier- und Pflanzengiften hitzebeständig. Es ist wahrscheinlich das stärkste bekannte natürliche Gift, das nicht wie ein Peptid aus Aminosäuren besteht.
Wirkung
[Bearbeiten | Quelltext bearbeiten]Mit einer letalen Dosis (LD50) von 50 Nanogramm pro Kilogramm Körpergewicht i.p. in Mäusen gehört Maitotoxin-1 zu den giftigsten natürlich vorkommenden Substanzen. Die toxische Wirkung beruht auf einer Aktivierung von calciumdurchlässigen, nichtselektiven Kationenkanälen in der Zellmembran. Dadurch kommt es zu einem massiven Einstrom von Calciumionen in das Cytosol der Zellen und damit einer Störung des Elektrolytgleichgewichts der Zellen im Körper. Darüber hinaus verursacht es Kontraktionen der glatten Muskulatur und die Freisetzung von Neurotransmittern.
Synthese
[Bearbeiten | Quelltext bearbeiten]Seit 1996 beschäftigt sich die Arbeitsgruppe von K. C. Nicolaou mit der Totalsynthese,[6][7][8][9] wenngleich das Projekt momentan ruht, weil es Probleme mit der Finanzierung gibt.[10]
Literatur
[Bearbeiten | Quelltext bearbeiten]- T. Yasumoto: The Chemistry and Biological Function of Natural Marine Toxins. In: The Chemical Record. 1(3)/2001. Wiley, S. 228–242, doi:10.1002/tcr.1010, PMID 11895121.
- L. I. Escobar, C. Salvador, M. Martinez, L. Vaca: Maitotoxin, a Cationic Channel Activator. In: Neurobiology (Bp). 6(1)/1998. Akadémiai Kiadó, S. 59–74, PMID 9713832.
- Yoshito Kishi: Complete Structure of Maitotoxin. In: Pure and Applied Chemistry. 70(2)/1998. IUPAC, S. 339–344, doi:10.1351/pac199870020339.
- A. Yokoyama, M. Murata, Y. Oshima, T. Iwashita, T. Yasumoto: Some Chemical Properties of Maitotoxin, a Putative Calcium Channel Agonist Isolated From a Marine Dinoflagellate. In: Journal of Biochemistry (Tokyo). 104(2)/1988. Japanese Biochemical Society, S. 184–187, doi:10.1093/oxfordjournals.jbchem.a122438, PMID 3182760.
- Michael Weiß: Pharmakologie und Toxikologie von Maitotoxin und anderen marinen Toxinen (PDF-Datei; 3,5 MB). Abschlussarbeit des Postgradualstudiums Toxikologie und Umweltschutz an der Medizinischen Fakultät der Universität Leipzig, 2001, S. 24–30.
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b Akihiro Yokoyama, Michio Murata, Yasukatsu Oshima, Takashi Iwashita, Takeshi Yasumoto: Some Chemical Properties of Maitotoxin, a Putative Calcium Channel Agonist Isolated from a MarineDinoflagellate1. In: The Journal of Biochemistry. Band 104, Nr. 2, 1988, S. 184–187, doi:10.1093/oxfordjournals.jbchem.a122438.
- ↑ Für diesen Stoff liegt noch keine harmonisierte Einstufung vor. Wiedergegeben ist eine von einer Selbsteinstufung durch Inverkehrbringer abgeleitete Kennzeichnung von Maitotoxin im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 13. August 2018.
- ↑ Eintrag zu Maitotoxin in der ChemIDplus-Datenbank der United States National Library of Medicine (NLM), abgerufen am 13. August 2018. (Seite nicht mehr abrufbar)
- ↑ Toshiyuki Hamada, Shigeki Matsunaga, Gen Yano, Nobuhiro Fusetani: Polytheonamides A and B, Highly Cytotoxic, Linear Polypeptides with Unprecedented Structural Features, from the Marine Sponge, Theonella swinhoei. In: Journal of the American Chemical Society. Band 127, Nr. 1, 2005, S. 110–118, doi:10.1021/ja045749e.
- ↑ Makoto Sasaki, Nobuaki Matsumori, Takahiro Maruyama, Taro Nonomura, Michio Murata, Kazuo Tachibana, Takeshi Yasumoto: The Complete Structure of Maitotoxin, Part I: Configuration of the C1–C14 Side Chain. In: Angewandte Chemie International Edition. Band 35, Nr. 15, 1996, S. 1672–1675, doi:10.1002/anie.199616721.
- ↑ Nicolaou, K. C., Cole, Kevin P., Frederick, Michael O., Aversa, Robert J. and Denton, Ross M. (2007), Chemical Synthesis of the GHIJK Ring System and Further Experimental Support for the Originally Assigned Structure of Maitotoxin. Angew. Chem. Int. Ed., 46: 8875–8879. doi:10.1002/anie.200703742
- ↑ Chemical Synthesis of the GHIJKLMNO Ring System of Maitotoxin K. C. Nicolaou, Michael O. Frederick, Antonio C. B. Burtoloso, Ross M. Denton, Fatima Rivas, Kevin P. Cole, Robert J. Aversa, Romelo Gibe, Taiki Umezawa, and Takahiro Suzuki Journal of the American Chemical Society 2008 130 (23), 7466–7476 doi:10.1021/ja801139f
- ↑ Synthesis of the ABCDEFG Ring System of Maitotoxin K. C. Nicolaou, Robert J. Aversa, Jian Jin, and Fatima Rivas Journal of the American Chemical Society 2010 132 (19), 6855-6861 doi:10.1021/ja102260q
- ↑ Synthesis and Biological Evaluation of QRSTUVWXYZA′ Domains of Maitotoxin K. C. Nicolaou, Philipp Heretsch, Tsuyoshi Nakamura, Anna Rudo, Michio Murata, and Keiichi Konoki Journal of the American Chemical Society Article 2014 ASAP doi:10.1021/ja509829e
- ↑ Chemistry's toughest total synthesis challenge put on hold by lack of funds. Katrina Kramer, 15. Januar 2015, Chemistry World.
